P8
Die Renin- Angiotensin-II-Achse: ein neuartiges Ziel für die Behandlung akuter Nierenschäden
Zusammenfassung
Die Entwicklung einer AKI erschwert die Behandlung von Sepsis und systemischen Entzündungen erheblich und ist mit ungünstigen gesundheitlichen Folgen verbunden. Jüngste epidemiologische Studien haben gezeigt, dass selbst milde oder kurze Episoden von AKI bei Überlebenden einer Sepsis ein höheres Risiko für die Entwicklung einer chronischen Nierenerkrankung im Endstadium im späteren Leben mit sich bringen. Klinische Therapieansätze um ein AKI zu verhindern waren bisher weitgehend erfolglos. Bisherige klinische Therapieansätze setzen zumeist erst nach einem AKI-Ereignis an, wenn bereits eine Verschlechterung der Nierenfunktion (d. h. der glomerulären Filtrationsrate) evident ist. Die Verabreichung von Noradrenalin gilt derzeit als Therapie der ersten Wahl zur Behandlung der Vasoplegie. Alle Katecholamine haben jedoch auch unerwünschte Wirkungen, darunter Myokardischämie und Herzrhythmusstörungen. In einer kürzlich durchgeführten Beobachtungsstudie konnten wir eine Dysregulation des Renin-Angiotensin-Aldosteron-Systems (RAAS) nachweisen, die wahrscheinlich auf eine verminderte Aktivität des Angiotensin-konvertierenden Enzyms (ACE) nach einer Herzoperation zurückzuführen ist.
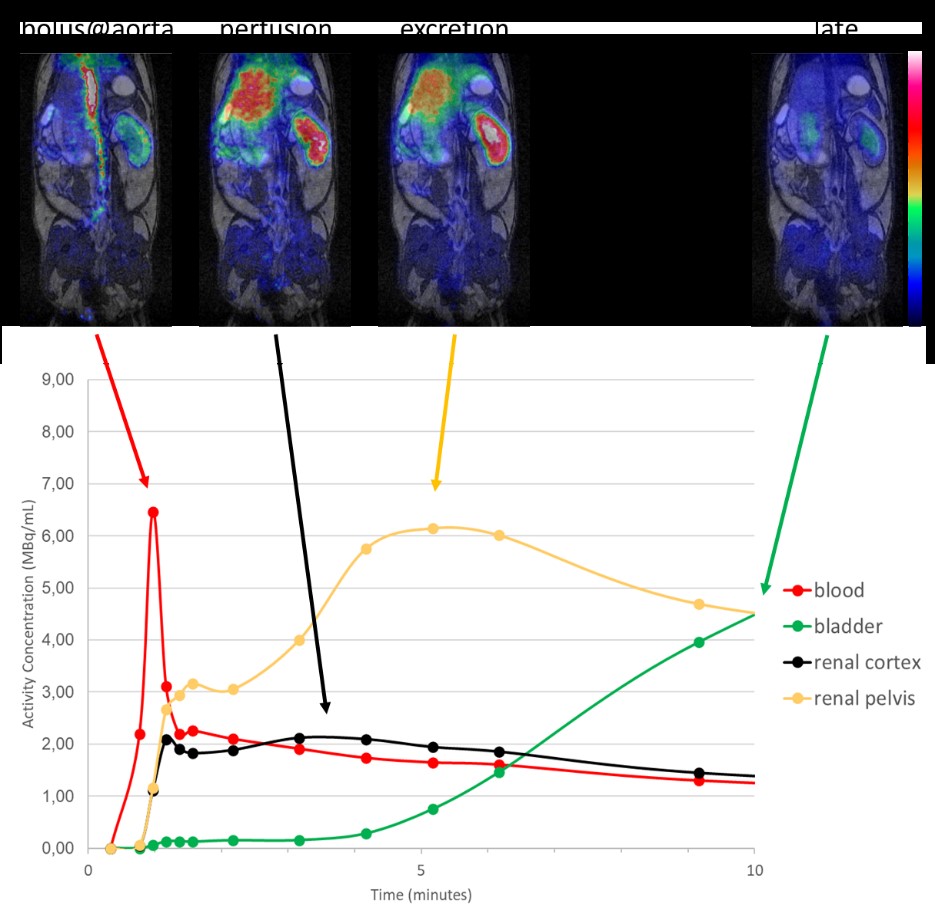
Dynamische Ganzkörper-[18F]-FDG-PET-MRI bei Mäusen
In diesem Projekt untersuchen wir, ob die Gabe von Angiotensin II die AKI-Pathogenese verbessert, indem es sowohl die Regulierung der Mikrohämodynamik und der glomerulären Filtration als auch die Entzündungsreaktion in der Niere moduliert. Multiskalige und translationale Bildgebungsansätze, die von der Intravitalmikroskopie bis zur funktionellen/metabolischen und AT1-Rezeptor-Ganzkörperbildgebung reichen, werden etabliert und angewandt, um die regionale Nierendurchblutung, Funktion und Entzündung sowie die AT-Rezeptordichte während des Krankheitsverlaufs und nach Angiotensin-II-Gabe zu korrelieren.



